北京大学团队开发荧光偶极子三维取向映射显微技术
- 2024-05-17 09:03:1230353
来源:北京大学
由于细胞的高度透明性,观察其中的细胞器十分困难。通过荧光染色,生物学家可以标记特定的细胞器对其进行观察。绝大部分荧光分子在吸收或发射过程中,表现为有方向的偶极子。通过荧光偏振显微镜测量偶极子特性,能够反映靶分子的取向特性,从而为研究靶分子的空间构象和运动特性提供重要信息。
为了打破传统荧光偏振显微镜受光学衍射限制的问题,诸多超分辨荧光偏振显微镜技术被提出,如单分子定向定位显微镜(SMOLM)和偏振调制技术(SDOM、SPoD等)。然而,SMOLM在追求高空间分辨率的同时牺牲了时间分辨率,使得快速生物成像成为一项艰巨的挑战。SDOM等偏振调制技术虽具有较高的时空分辨率,但只能求解偶极子的二维取向,缺乏解析偶极子三维取向的能力。三维取向能够提供荧光分子更全面的三维空间结构,因此,关键问题是如何打破时空分辨率和取向维度之间的权衡,实现超过衍射极限分辨率的同时,能够快速成像和解析偶极子的三维方向。
针对偶极子取向解析问题,北京大学未来技术学院席鹏教授团队继2016年提出二维偶极子取向映射方法SDOM(Light.: Sci. Appl., 2016),及2022年基于光学锁相探测的二维取向映射方法OLID-SDOM(Light.: Sci. Appl., 2022)后,为打破时空分辨率和三维取向维度的权衡瓶颈,开发了新型的三维取向映射显微镜(3DOM)。相关研究成果以“Three-dimensional dipole orientation mapping with high temporal-spatial resolution”为题,于2024年4月16日在线发表在PhotoniX期刊。
3DOM方法基于团队开发的偏振结构光超分辨显微技术,把杨氏双缝干涉的原理反过来,结合光路可逆的原理,利用不同角度的条纹产生不同方向的正负一级光束。进一步,只需要把相应的负一级次光挡住,就可以产生单一方向的倾斜照明。把这一倾斜投影到z轴不同的角度,利用FISTA算法对图像进行重建,在倒易空间结合偏振调制系数和重建结果,即可实现高精度的偶极子取向解析。
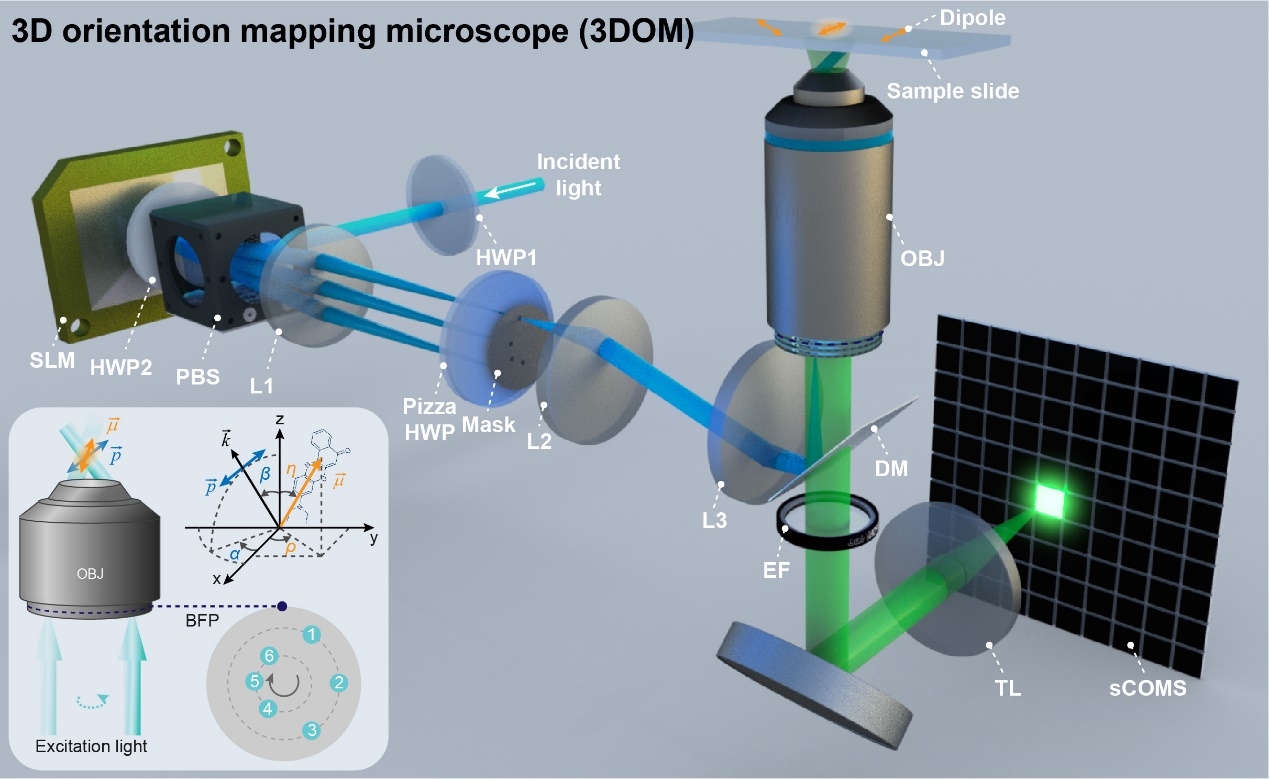
图1 三维取向映射显微镜原理图

图2 SYTOX Orange标记λ-DNA的3DOM成像结果
研究结果表明,3DOM方法有效地克服了偏振荧光显微镜在使用宽场成像进行高时空分辨率和三维方向映射方面的局限性,提供了更全面的荧光团分子的三维空间结构。这不仅能够应用于区分DNA、膜细胞器以及各种细胞骨架组织的宏观形态(肌动蛋白丝和微管),而且还可以获得结构的有序性和结合紧密度等有价值的信息。此外,3DOM的主要优点之一是它易于在现有的宽场系统中升级,适用范围广,这增强了其在不同研究环境中的可及性和可用性。可以预见未来3DOM这个强大的工具将会有助于研究人员解析复杂的细胞器结构,推动对众多生物结构和纳米级相互作用的理解,为结构生物学家、生物动力学家带来新的观察工具。
席鹏和生命科学学院李美琪老师为本文的共同通讯作者。北京大学未来技术学院博士生钟素艺为该项成果的第一作者。该研究得到了科技部国家重点研发计划、国家自然科学基金等项目的支持。
席鹏课题组致力于发展新型超分辨显微成像技术,在偏振超分辨方面开展了如下工作:(1)利用偏振偶极子解析实现了50nm的超分辨与荧光二维偶极子测量(Light: Science and Applications 2016 ); (2)通过解析结构光超分辨中的偏振信息,实现了偏振SIM超分辨(Nature Communications 2019),并成功实现商业化;(3)结合荧光分子的化学极性(光谱红移)与物理序性(偶极子自由度)信息,成功实现了10种细胞器的同时观察与环境研究(Nature Communications 2020);(4)通过偏振调制和光学锁定放大技术来增强微弱的偏振调制信号,实现活细胞中亚细胞结构的荧光各向异性的高灵敏度测量(Light: Science and Applications 2022);(5)发展了具有偶极子方位解析能力的3D-SIM开源软件Open-3DSIM(Nature Methods 2023 )和开源硬件(Advanced Photonics Nexus 2024);(6)对相关的SIM重建算法进行了系统综述(Light: Science and Applications 2023) 。